
dr hab. Ewa Kłodzińska
Biegły sądowy z zakresu badań chemicznych i kryminalistycznych przy SO w Warszawie,
specjalista chemii analitycznej, technik separacyjnych i diagnostyki medycznej, dietetyk kliniczny Instytut Medycyny Innowacyjnej Sp z o.o,, Klinika Długowieczności-Kierownik Pracowni Zaburzeń Odżywiania Komórkowego i Aktywności Komórek Macierzystych, Kraków
Prezes EK Bio-Med Sp. z o.o.
1. Wprowadzenie: dlaczego biodostępność glutationu ma znaczenie
GSH (γ‐glutamylocysteinyloglicyna) neutralizuje reaktywne formy tlenu/azotu, regeneruje wit. C/E i jest sprzęgany z ksenobiotykami przez transferazy GST, co ułatwia ich wydalanie [1,2]. Zaburzenia gospodarki GSH to wspólny mianownik wielu chorób przewlekłych (neurodegeneracja, miażdżyca, cukrzyca, przewlekły stan zapalny) [1,2,23].
Skuteczność suplementacji ograniczają bariery farmakokinetyczne: degradacja w jelitach (γ‐glutamylotransferaza), niekorzystny transport przez nabłonek oraz efekt pierwszego przejścia [30]. Stąd rozwój systemów nośnikowych (liposomy, nanoemulsje), dróg alternatywnych (transdermalnie, inhalacyjnie), metod indukujących endogenny GSH (PBM) i podań pozajelitowych.
2. Doustny glutation: „klasyczne” kapsułki/tabletki
Przez wiele lat uważano, że glutation doustny nie podnosi poziomów ustrojowych z powodu rozkładu enzymatycznego. Późniejsze badania skorygowały ten pogląd: w RCT Richie i wsp. (6 mies., 250–1000 mg/d, zdrowi dorośli) stwierdzono wzrost puli GSH w erytrocytach, limfocytach i osoczu oraz korzystne zmiany markerów stresu oksydacyjnego [4]. Klinicznie istotne efekty obserwuje się też w dermatologii (przebarwienia/melasma), choć rezultaty pozostają umiarkowane i zależne od dawki, czasu i populacji [5]. Wniosek: klasyczny doustny GSH działa, ale przeciętnie — i z reguły słabiej niż formy udoskonalone technologicznie [3–5,23].
3. Doustny liposomalny i nanoemulsje (w tym płynne nanoemulsje typu „Neumi”)
Celem tej technologii jest ochronina GSH przed hydrolizą i ułatwienie przenikania przez błony, zwiększając biodostępność. Liposomy i nanoemulsje „otulają” cząsteczkę fosfolipidami/surfaktantami, stabilizując ją i poprawiając absorpcję [5]. W badaniu Sinha i wsp. u zdrowych ochotników dwutygodniowa suplementacja liposomalnym GSH istotnie podniosła zasoby GSH (osocze, RBC), zwiększyła aktywność komórek NK i poprawiła wskaźniki redoks [3]. Równolegle liczne prace przeglądowe/technologiczne potwierdzają przewagi stabilności i przenikania nano‐nośników wobec proszków/kapsułek [5,25,26].
Płynne nanoemulsje (kategoria, do której należy m.in. Neumi — forma płynna) teoretycznie zwiększają kontakt z błoną śluzową jamy ustnej i przyspieszają wchłanianie. Prace o wchłanianiu orobukkalnym GSH sugerują szybki transfer i sens tej drogi [6]. Dla konkretnych marek płynnych nanoemulsji wciąż brakuje dużych, niezależnych RCT; jednak mechanistycznie i farmakokinetycznie jest to spójne z danymi dla liposomalnego GSH [3,5,6].
W praktyce: jeśli celem jest wzrost puli GSH w krążeniu i funkcjonalny efekt biologiczny, liposomalne/nanoemulsje są obecnie najlepiej udokumentowaną doustną alternatywą (kompromis między wygodą, kosztami i efektami) [3,5].
4. Transdermalne systemy: plastry, mikronakłuwanie, niosomy/transferosomy
Celem wprowadzania tego typu systemów jest ominięcie przewodu pokarmowego i zapewnienie powolnego i stabilnego uwalnianie. Badania nad GSH w mikronakłuwających systemach transdermalnych pokazują, że możliwe jest miejscowe dostarczenie GSH, efekty kosmetyczne (rozjaśnienie) i poprawa wybranych parametrów redoks skóry przy dobrej tolerancji [14]. Szersze przeglądy TDD i mikronakłuć wskazują na istotny wzrost penetracji oraz możliwość formuł o przedłużonym działaniu [15–17]. Niosomy/transferosomy poprawiają dyfuzję przez warstwę rogową, co może mieć znaczenie dla małych hydrofilowych peptydów [18,26].
Co już wiemy klinicznie? Standardów jeszcze brak; najwięcej danych dotyczy zastosowań dermatologicznych (kosmetologia, przebarwienia) i sytuacji wymagających efektu miejscowego, a potencjalnie — przy dalszych badaniach — wsparcia systemowego.
5. Fotobiomodulacja (PBM): zwiększanie endogennej syntezy GSH
PBM (światło czerwone/nIR) aktywuje łańcuch oddechowy (m.in. kompleks IV), co może zwiększać syntezę endogennego GSH i poprawiać równowagę redoks w tkankach [9,10].
Badania in vitro, przeglądy i metaanalizy potwierdzają spadek markerów stresu oksydacyjnego i poprawę wyników funkcjonalnych w różnych modelach klinicznych [9–12]. Znaczenie gospodarki GSH jest podkreślane również w narządach wysokiego stresu oksydacyjnego (np. oko) [13].
Rola w praktyce: PBM nie „dostarcza” GSH, ale wspiera jego szlaki. Sensowne jako terapia łączona z suplementacją w stanach przewlekłego stresu oksydacyjnego i dysfunkcji mitochondriów.
6. Inhalacyjny (donosowy/dooskrzelowy) GSH
W mukowiscydozie randomizowane badania wykazały poprawę funkcji płuc i redukcję nasilenia zapalenia po wziewnym GSH [19,20]; wcześniejszy pilotaż potwierdził bezpieczeństwo i sygnał skuteczności [21]. Droga donosowa była testowana m.in. w chorobie Parkinsona (MRS, fazy I–II), wskazując na możliwość zwiększenia GSH w OUN — szerzej o roli GSH w parkinsonizmie piszą aktualne przeglądy [22].
Wnioski praktyczne: inhalacja zapewnia wysokie stężenia lokalne (drogi oddechowe), ale efekt systemowy jest ograniczony; zastosowanie powinno być wskazaniowo specyficzne.
7. Dożylny GSH
Ta droga podania daje 100% biodostępności i szybki efekt, co tłumaczy jej popularność w praktykach integracyjnych i wybranych protokołach klinicznych [23,30]. W neurologii i hepatologii GSH pozostaje ważnym celem biologicznym, choć dla wielu wskazań brak dużych, dobrze zaprojektowanych RCT; efekty bywają krótkotrwałe, co wymaga powtarzanych infuzji [22,23,30].
Plusy/minusy: najwyższa biodostępność i szybki efekt kontra konieczność procedur medycznych, koszty i ograniczenia logistyczne.
8. Dieta i endogenny „recykling” GSH
`Wsparcie dietetyczne (prekursory siarki, cysteina/NAC, wybrane fitoskładniki) ułatwia syntezę i recykling GSH — aktualny przegląd podsumowuje najważniejsze (phyto)nutrienty i strategie żywieniowe [28]. Znaczenie enzymów GPX w ochronie przed stresem oksydacyjnym i regulacjach adaptacyjnych podkreślają świeże prace przeglądowe [24]. Na horyzoncie badań translacyjnych znajduje się oś GSH–ferroptoza jako potencjalny cel onkologiczny [27].
9. Fakty i mity
✅ Fakty
-
GSH to centralny bufor redoks i kofaktor detoksykacji; jego niedobór koreluje z wieloma chorobami przewlekłymi [1,2,23].
-
Biodostępność zależy od drogi podania: dożylny > liposomalny/nanoemulsje ≥ (inhalacyjny – lokalnie) > doustny klasyczny; PBM i transdermalne to drogi pośrednie/wspierające [3–5,9–21].
-
Nanoformy (liposomalne, nanoemulsje) to najlepszy kompromis „wygoda × efekt” w warunkach ambulatoryjnych [3,5].
❌ Mity
-
„Wszystkie formy GSH działają tak samo” — nieprawda; różnice biodostępności są zasadnicze [3–5,19–21].
-
„Klasyczny doustny GSH nic nie daje” — może działać, ale zwykle słabiej i wymaga dłuższej/właściwej dawki [4,5].
-
„Transdermalne i PBM mają dowody jak i.v.” — nie; to obiecujące strategie, lecz potrzebują dużych, niezależnych RCT [11,14–17].
10. Materiały producentów:
10.1. LifeWave® – plastry „Glutathione”
Zestaw raportów klinicznych (PDF „Y‐Age® Glutathione Clinical Studies”): zebrane małe badania (2006–2010), głównie otwarte; m.in.:
✓ 40 osób z trądzikiem (6 tyg., równolegle z homeopatycznym sprayem; brak grupy placebo; oceny dermatologiczne w 1.–6. tyg.).
✓ 30 zdrowych (4 tyg., otwarte) — pomiary „funkcji narządów” za pomocą Electro‐Interstitial Scan (EIS); wzrost „statusu fizjologicznego” w 7–8 narządach przy noszeniu 12 h/d [p < 0,001 dla wielu punktów]; brak klasycznych markerów biochemicznych.
✓ 9 zdrowych (otwarte, LabCorp, 15 dni) — pomiary GSH we krwi w wielokrotnych punktach; raport: wzrosty średnio > 2,6‐krotnie względem linii bazowej; zmienność osobnicza; wtórnie: wydalanie Hg w moczu u części badanych; bez korelacji z GSH.
✓ 15 osób (otwarte, 5 dni) — codzienne pomiary GSH w pełnej krwi; wzrosty u wszystkich; część wyników osiągała górną granicę wykrywalności testu.
✓ Randomizowane, podwójnie ślepe (Pune, Indie; PIP/GDV/EIS jako metody „bioenergetyczne”, 50 + 50 + 20 kontrola) — brak klasycznych punktów biochemicznych; poprawa parametrów „energetycznych” ~80% badanych.
Działania niepożądane: zgłaszano drobny świąd pod plastrem; poważnych zdarzeń brak.
Kluczowe ograniczenia: małe próby, często brak grupy placebo/blind, nie‐kliniczne metody oceny (EIS, PIP, GDV), współstosowane produkty (spray) → niska wiarygodność kliniczna, brak publikacji z IF.
Uwaga bezpieczeństwo: w bazie FDA MAUDE notowano pojedyncze zgłoszenia zdarzeń niepożądanych związanych z „LifeWave Glutathione/X39 patch” (zgłoszenie 2023; charakter opisowy, sygnałowy; nie dowód przyczynowy).
10.2. Neumi® – płynna nanoemulsja („NutriSwish/Neumi Skin”)
Producent udostępnia white papers i stronę „About the Science”, opisując HydraStatTM nano‐enkapsulację i „zwiększoną biodostępność” (brak pełnych danych farmakokinetycznych: bez RCT opublikowanych w czasopismach z IF; brak rejestrów ClinicalTrials z zakończonymi badaniami Neumi‐specyficznymi). Dokumenty powołują się na ogólne piśmiennictwo o glutationie i nanotechnologii, bez prezentacji pełnych protokołów, randomizacji, punktów końcowych i analizy statystycznej dla własnego produktu.
Przejrzystość: materiały Neumi są marketingowo‐edukacyjne; należy je traktować jako hipotezy technologiczne zgodne z wiedzą o nanoemulsjach, ale niewystarczające jako dowód klinicznej skuteczności konkretnego produktu bez niezależnych RCT.
10.3. Quicksilver Scientific® – liposomalny GSH (płyn)
Strona produktu podaje wynik wewnętrznego, 4‐tygodniowego badania: +25% całkowitego glutationu w surowicy po 250 mg BID; próbki analizował zewnętrzny lab (Precision Point Diagnostics). Brak pełnego opisu protokołu, randomizacji i grupy kontrolnej; dane nieopublikowane w czasopiśmie z IF.
Firma prowadzi CLIA‐certyfikowane laboratorium diagnostyczne (np. Mercury Tri‐Test w kontekście detoksykacji), co świadczy o zapleczu analitycznym, choć nie zastępuje RCT skuteczności suplementów.
Niezależnie od materiałów firmowych, liposomalny GSH jako klasa ma wsparcie danych klinicznych (Sinha 2018 RCT u zdrowych) — ale to nie jest badanie Quicksilver per se [3].
11. Zastosowania praktyczne i algorytm wyboru formy
Cel: szybki i silny efekt systemowy - GSH (klinika; krótki czas działania; rozważyć plan infuzji) [23,30].
Cel: długofalowe wsparcie redoks/detoksykacji ambulatoryjnie - liposomalny/nanoemulsje (lepszy kompromis biodostępność/wygoda/koszt) [3,5].
Cel: dermatologia/kosmetologia, działanie miejscowe - transdermalne/mikronakłuwanie; narzędzia obiecujące, wymagają standaryzacji i RCT [14–18,26].
Cel: wsparcie endogennej syntezy i mitochondriów - PBM jako terapia uzupełniająca [9–12].
Cel: drogi oddechowe (CF i inne wskazania pulmonologiczne) - inhalacyjny GSH (dowody kliniczne dla CF) [19–21].
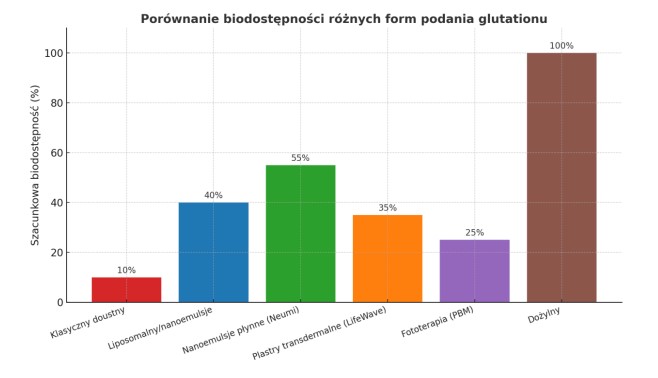
Rys. 1. Porównanie biodostępności różnych form podania glutationu.
12. Podsumowanie
-
Nie wszystkie formy GSH są równoważne — różnią się biodostępnością, dynamiką efektu i jakością dowodów klinicznych.
-
Najsilniejszy efekt systemowy: podawanie dożylne w warunkach klinicznych.
-
Najlepszy kompromis ambulatoryjny: formy liposomalne/nanoemulsje (wygoda × skuteczność).
-
Transdermalne i PBM: biologicznie zasadne, ale wymagają dużych, niezależnych badań RCT, by potwierdzić skuteczność.
ℹ️ Ważne zastrzeżenie
Materiały producentów (Neumi, LifeWave, Quicksilver) dostarczają wstępnych lub marketingowych danych.
👉 Decyzje kliniczne powinny opierać się przede wszystkim na recenzowanej literaturze naukowej z DOI, przytoczonej w bibliografii poniżej.
Wyjaśnienie
Termin RTC - oznacza Randomized Controlled Trial, czyli randomizowane badanie kliniczne z grupą kontrolną – tzw. „złoty standard” w ocenie skuteczności terapii i suplementów.
W takich badaniach uczestnicy są losowo przydzielani do grupy interwencyjnej (np. suplementacja glutationem) albo kontrolnej (placebo / standardowa terapia), randomizacja minimalizuje błędy systematyczne i wpływ czynników zakłócających, analizuje się różnice efektów zdrowotnych między grupami. Jeśli w publikacji widzisz np. „double-blind RTC”, oznacza to podwójnie ślepe randomizowane badanie kliniczne – ani pacjenci, ani badacze nie wiedzą, kto otrzymuje substancję czynną, a kto placebo.
Bibliografia
1. Vašková J, Kočan L, Vaško L, Perjési P. Glutathione‐Related Enzymes and Proteins: A Review. Molecules. 2023;28(3):1447. doi:10.3390/molecules28031447
2. Giustarini D, Dalle‐Donne I, Milzani A, Colombo R, Rossi R. How to Increase Cellular Glutathione. Antioxidants (Basel). 2023;12(5):1094. doi:10.3390/antiox12051094
3. Sinha R, Sinha I, Calcagnotto A, et al. Oral supplementation with liposomal glutathione elevates body stores of glutathione and markers of immune function. Eur J Clin Nutr. 2018;72(1):105‐111. doi:10.1038/ejcn.2017.132
4. Richie JP Jr, Nichenametla S, Neidig W, et al. Randomized controlled trial of oral glutathione supplementation on body stores of glutathione. Eur J Nutr.
2015;54(2):251‐263. doi:10.1007/s00394‐014‐0706‐z
5. Sarkar R, Arora P, Garg VK, Sonthalia S, Gokhale N, et al. Randomized, double‐blind, placebo‐controlled trial of oral reduced and oxidized glutathione in melasma. Int J
Dermatol. 2024;63(6):711‐719. doi:10.1111/ijd.17535
6. Sitohang IBS, Pratiwi FD, Sari IP. Augmented Glutathione Absorption from Oral Mucosa. Dermatol Res Pract. 2020;2020:8547960. doi:10.1155/2020/8547960
7. Mischley LK, Conley KE, Shankland EG, et al. Central nervous system uptake of intranasal glutathione in Parkinson’s disease. npj Parkinsons Dis. 2016;2:16002. doi:10.1038/npjparkd.2016.2
8. Mischley LK, Lau RC, Shankland EG, et al. Phase IIb Study of Intranasal Glutathione in Parkinson’s Disease. J Parkinsons Dis. 2017;7(2):289‐299.
doi:10.3233/JPD‐161040
9. Heo JY, et al. Photobiomodulation prevents oxidative stress and mitochondrial dysfunction in human cells. Sci Rep. 2019;9:6625. doi:10.1038/s41598‐019‐46490‐4
10. Salehpour F, et al. Transcranial photobiomodulation therapy: a narrative review. Front Neurosci. 2019;13:819. doi:10.3389/fnins.2019.00819
11. Pan MK, et al. Photobiomodulation modulates peripheral biomarkers and clinical outcomes: meta‐analysis. J Transl Med. 2023;21:504.
doi:10.1186/s12967‐023‐03988‐w
12. Lim WS, et al. Photobiomodulation in traumatic brain injury: mechanisms and clinical translation. Cells. 2024;13(5):385. doi:10.3390/cells13050385
13. Lim JC, et al. Redox Homeostasis in Ocular Tissues: Circadian Regulation and the Role of Glutathione. Antioxidants (Basel). 2022;11(8):1516.
doi:10.3390/antiox11081516
14. Lee Y, Kumar S, Kim SH, et al. Odorless Glutathione Microneedle Patches for Skin Whitening. Pharmaceutics. 2020;12(2):100. doi:10.3390/pharmaceutics12020100
15. Jeong WY, Kwon S, Choi HE, et al. Recent advances in transdermal drug delivery systems: A review. Biomater Res. 2021;25:24. doi:10.1186/s40824‐021‐00226‐6
16. Vora LK, Sabri AH, Naser Y, et al. Long‐acting microneedle formulations. Adv Drug Deliv Rev. 2023;201:115055. doi:10.1016/j.addr.2023.115055
17. Zhang J, Li H, Albakr L, et al. Microneedle‐enabled therapeutics delivery and biosensing in clinical trials. J Control Release. 2023;360:687‐704.
doi:10.1016/j.jconrel.2023.07.023
18. Alkilani AZ, Abdallah OY, et al. Microneedles loaded with antioxidant niosomes for dermal delivery. Pharmaceutics. 2023;15(10):2444.
doi:10.3390/pharmaceutics15102444
19. Griese M, Kappler M, Eismann C, et al. Inhalation treatment with glutathione in cystic fibrosis: A randomized clinical trial. Am J Respir Crit Care Med. 2013;188(1):83‐89. doi:10.1164/rccm.201303‐0427OC
20. Calabrese C, Tosco A, Abete P, et al. Randomized, single‐blind, controlled trial of inhaled glutathione vs placebo in cystic fibrosis. J Cyst Fibros. 2015;14(2):203‐210. doi:10.1016/j.jcf.2014.09.014
21. Bishop C, Hudson VM, Hilton SC, Wilde C. A pilot study of inhaled buffered reduced glutathione in cystic fibrosis. Chest. 2005;127(1):308‐317.
doi:10.1378/chest.127.1.308
22. Asanuma M, Miyazaki I. Glutathione and Related Molecules in Parkinsonism. Int J Mol Sci. 2021;22(16):8689. doi:10.3390/ijms22168689
23. Santacroce L, Charitos IA, et al. Glutathione: Pharmacological Aspects and Implications in Pathology. Front Med (Lausanne). 2023;10:1124275.
doi:10.3389/fmed.2023.1124275
24. Pei J, et al. Research progress of glutathione peroxidase family (GPX) in oxidative stress. Front Pharmacol. 2023;14:1147414. doi:10.3389/fphar.2023.1147414
25. Chen Y, Zhang J, et al. A bibliometric and visualized analysis of transdermal drug delivery (2003–2022). Front Pharmacol. 2023;14:1173251.
doi:10.3389/fphar.2023.1173251
26. Matharoo N, Kheraj T, et al. Transferosomes as a transdermal drug delivery system. WIREs Nanomed Nanobiotechnol. 2024;16(1):e1918. doi:10.1002/wnan.1918
27. Jiang Y, Glandorff C, Sun M. GSH and ferroptosis: partners against tumors. Antioxidants (Basel). 2024;13(6):697. doi:10.3390/antiox13060697
28. Minich DM, Brown BI. A Review of Dietary (Phyto)Nutrients for Glutathione Support. Nutrients. 2019;11(9):2073. doi:10.3390/nu11092073
29. Lee KH, et al. Photobiomodulation and sleep: mechanisms and clinical evidence. Sleep Med Res. 2024;15(1):1‐15. doi:10.17241/smr.2024.02593
30. Lu SC. Glutathione in Liver Injury and Disease: Therapeutic Potential and Mechanisms. Pharmacol Ther. 2019;198:67‐77. doi:10.1016/j.pharmthera.2019.02.002
Materiały producentów (źródła firmowe; nie są to publikacje recenzowane)
LifeWave®:
1. Zbiorczy raport „Y‐Age® Glutathione Clinical Studies” (przegląd 6 małych badań: otwarte, pilotowe, z EIS/PIP/GDV; m.in. 40 osób z trądzikiem + spray; 30 zdrowych; 9 zdrowych z pomiarami LabCorp; 15 zdrowych 5 dni; 1 badanie rzekomo RCT z metodami „bioenergetycznymi”). Brak pełnych RCT z klasycznymi biomarkerami.
2. „Nanoscale Glutathione Patches Improve Organ Function” (EIS; poprawy „statusu narządów” po 4 tyg.; bez standardowych punktów końcowych).
3. Testy GDV/HRV (badania starsze, o charakterze eksploracyjnym).
4. Zgłoszenie sygnałowe MAUDE (FDA) dot. patchy (charakter opisowy).
Neumi®:
1. Strony „About the Science” i white papers dot. HydraStatTM (nano‐enkapsulacja; roszczenia dot. „zwiększonej biodostępności” bez publikacji RCT).
Quicksilver Scientific®:
1. Strona produktu z wewnętrznym 4‐tygodniowym badaniem (+25% GSH w surowicy przy 250 mg BID; lab zewnętrzny; brak randomizacji/kontroli).
2. Materiały o zapleczu analitycznym (CLIA lab; Mercury Tri‐Test).



