Dr hab. Ewa Kłodzińska
Wprowadzenie
Homocysteina jest siarkowym aminokwasem niebiałkowym, powstającym w organizmie człowieka jako pośredni metabolit cyklu metioninowego. W warunkach fizjologicznych jej stężenie we krwi utrzymywane jest na niskim poziomie dzięki sprawnie działającym szlakom remetylacji oraz transsulfuracji, zależnym przede wszystkim od dostępności witamin z grupy B: kwasu foliowego (B9), kobalaminy (B12) oraz pirydoksyny (B6). Zaburzenie tych szlaków prowadzi do hiperhomocysteinemii, która w ostatnich dekadach została jednoznacznie powiązana z ryzykiem chorób sercowo-naczyniowych, neurodegeneracyjnych, powikłań zakrzepowo-zatorowych, zaburzeń płodności, a także procesów przyspieszonego starzenia.
W klasycznej medycynie homocysteina oceniana jest jako parametr laboratoryjny w surowicy krwi. Diagnostyka funkcjonalna, w tym system SO/CHECK, pozwala natomiast uchwycić skutki podwyższonej homocysteiny na poziomie tkankowym, komórkowym i metabolicznym, zanim dojdzie do pełnoobjawowych zaburzeń klinicznych. Artykuł ten omawia biochemię homocysteiny, jej patofizjologiczne znaczenie oraz sposób, w jaki jej dysregulacja manifestuje się w analizie funkcjonalnej SO/CHECK.
Biochemia homocysteiny – cykl metioninowy i metabolizm jednowęglowy
Homocysteina powstaje w wyniku demetylacji metioniny, aminokwasu egzogennego dostarczanego z dietą. Metionina po aktywacji do S-adenozylometioniny (SAM) pełni rolę głównego donora grup metylowych w organizmie. Po oddaniu grupy metylowej SAM przechodzi w S-adenozylhomocysteinę (SAH), która następnie hydrolizowana jest do homocysteiny.
Homocysteina może zostać:
1. Zremetylowana do metioniny – proces zależny od:
- kwasu foliowego (5-MTHF),
- witaminy B12 (metylokobalamina),
- enzymu syntazy metioninowej.
2. Skierowana do transsulfuracji – prowadzącej do powstania cystationiny i cysteiny, z udziałem:
- witaminy B6,
- enzymów CBS i CGL.
Każde zaburzenie dostępności kofaktorów, aktywności enzymów lub integralności jelit (wchłanianie witamin) prowadzi do kumulacji homocysteiny.
Hiperhomocysteinemia – mechanizmy toksyczności
Podwyższona homocysteina wykazuje wielokierunkowe działanie patogenne. Jej toksyczność nie wynika wyłącznie z samego stężenia, lecz z wpływu na strukturę i funkcję komórek.
Na poziomie śródbłonka naczyniowego homocysteina indukuje stres oksydacyjny, obniża biodostępność tlenku azotu (NO) oraz uszkadza glikokaliks, prowadząc do dysfunkcji śródbłonka i zwiększonej adhezji płytek krwi. Mechanizm ten tłumaczy związek hiperhomocysteinemii z miażdżycą i zakrzepicą.
Na poziomie erytrocytów dochodzi do zmian ładunku powierzchniowego błony komórkowej, spadku elastyczności krwinek oraz pogorszenia mikrokrążenia. Zjawiska te są szczególnie dobrze widoczne w diagnostyce funkcjonalnej, gdzie nie mierzy się jedynie stężenia homocysteiny, lecz jej efekt biologiczny.
W układzie nerwowym homocysteina działa neurotoksycznie, nasilając ekscytotoksyczność glutaminianu, zaburzając metylację neuroprzekaźników i sprzyjając procesom neurodegeneracyjnym.
Cykl metioninowy jest centralnym elementem metabolizmu jednowęglowego, odpowiedzialnego za:
- metylację DNA i histonów,
- syntezę neuroprzekaźników,
- regulację ekspresji genów,
- prawidłową erytropoezę.
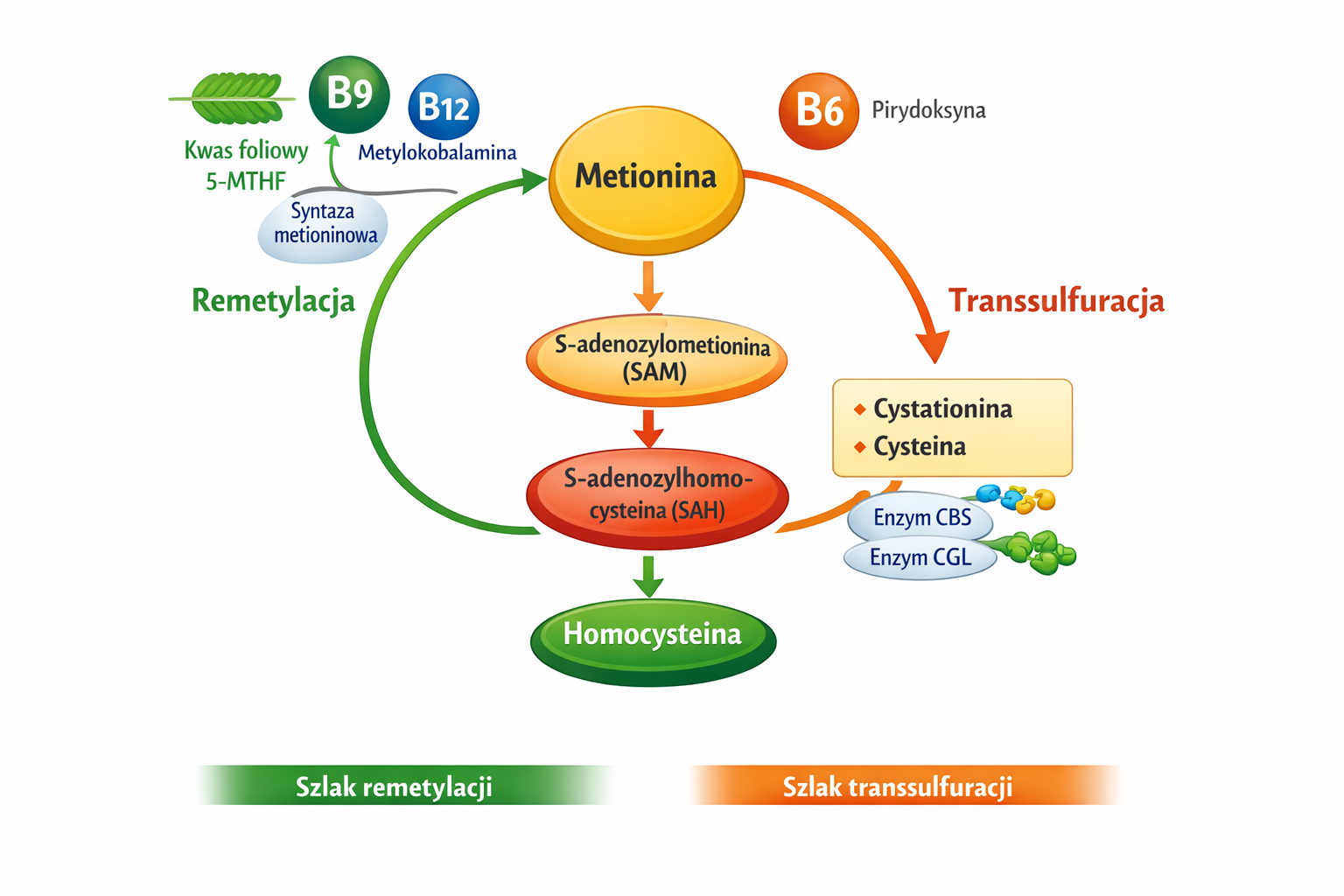
Rysunek 1.
Schemat metabolizmu homocysteiny w cyklu metioninowym. Homocysteina powstaje w wyniku demetylacji metioniny pośrednio przez S-adenozylometioninę (SAM) i S-adenozylhomocysteinę (SAH). Jej dalszy los obejmuje dwa główne szlaki metaboliczne: remetylację do metioniny, zależną od kwasu foliowego w formie 5-MTHF oraz witaminy B₁₂ (metylokobalaminy), oraz transsulfurację prowadzącą do powstania cystationiny i cysteiny, zależną od witaminy B₆ i aktywności enzymów CBS i CGL. Zaburzenia dostępności kofaktorów witaminowych lub aktywności enzymatycznej prowadzą do kumulacji homocysteiny i rozwoju hiperhomocysteinemii.
Wzrost homocysteiny oznacza funkcjonalny deficyt metylacji. Klinicznie może to manifestować się:
- przewlekłym zmęczeniem,
- zaburzeniami nastroju,
- anemią megaloblastyczną,
- zaburzeniami hormonalnymi,
- przyspieszonym starzeniem komórkowym.
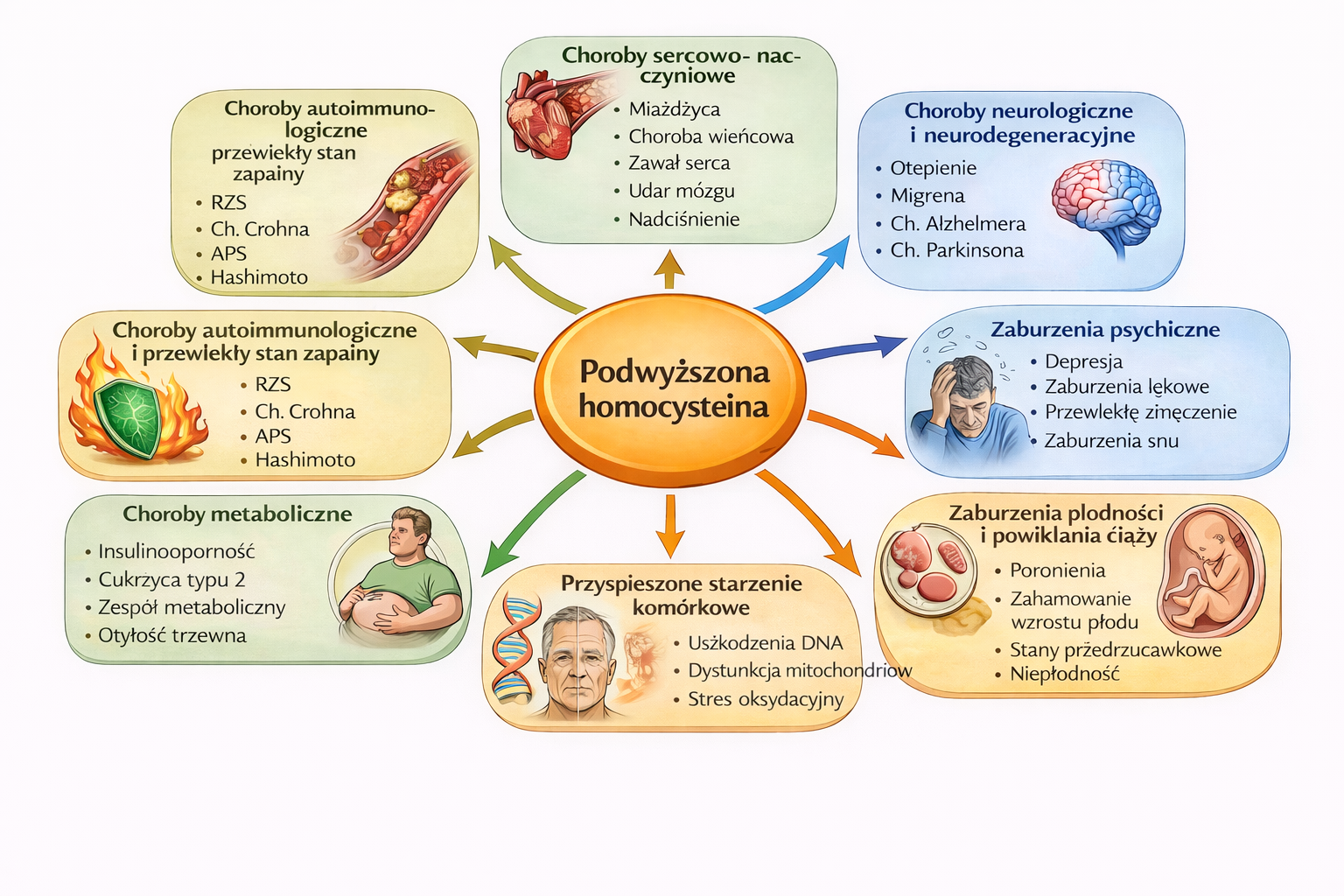
Rysunek 2.
Powiązania kliniczne podwyższonego stężenia homocysteiny. Hiperhomocysteinemia wiąże się z dysfunkcją śródbłonka naczyniowego i mikrokrążenia, nasileniem stresu oksydacyjnego oraz zaburzeniami procesów metylacji. Konsekwencją tych zmian jest zwiększone ryzyko chorób sercowo-naczyniowych i zakrzepowo-zatorowych, schorzeń neurologicznych i neurodegeneracyjnych, zaburzeń psychicznych, anemii megaloblastycznej, niepłodności i powikłań ciąży, osteoporozy, chorób autoimmunologicznych oraz zaburzeń metabolicznych, a także przyspieszonego starzenia komórkowego.
Manifestacja zaburzeń homocysteiny w diagnostyce SO/CHECK
System SO/CHECK nie mierzy homocysteiny bezpośrednio, lecz rejestruje jej funkcjonalne konsekwencje w tkankach. Charakterystyczny obraz obejmuje kilka współwystępujących obszarów.
Po pierwsze, obserwuje się niedobory funkcjonalne witamin B6, B9 i B12, często mimo prawidłowych lub granicznych wyników laboratoryjnych. Wynika to z zaburzonego wchłaniania jelitowego, stanu zapalnego jelit lub zwiększonego zapotrzebowania metabolicznego.
Po drugie, widoczny jest wzrost stresu oksydacyjnego, będący bezpośrednią konsekwencją działania homocysteiny na układ redoks komórki.
Po trzecie, w analizie erytrocytów pojawiają się cechy zaburzonego mikrokrążenia – obniżona elastyczność błon, zmiany potencjału powierzchniowego oraz wtórne objawy niedotlenienia tkanek.
Po czwarte, często towarzyszą temu zaburzenia fosforu i magnezu, odzwierciedlające upośledzoną produkcję ATP i spadek wydolności mitochondrialnej.
W praktyce klinicznej obraz SO/CHECK pozwala podejrzewać hiperhomocysteinemię nawet przed wykonaniem oznaczenia laboratoryjnego i ukierunkować dalszą diagnostykę.
Korelacje kliniczne – kiedy podejrzewać podwyższoną homocysteinę
Na podstawie obrazu funkcjonalnego szczególną czujność należy zachować u pacjentów z:
- chorobami sercowo-naczyniowymi,
- migrenami i zaburzeniami neurologicznymi,
- niepłodnością i poronieniami nawracającymi,
- osteoporozą,
- chorobami autoimmunologicznymi,
- przewlekłym zmęczeniem i depresją.
W tych grupach SO/CHECK często ujawnia charakterystyczną triadę: zaburzenia witamin B, stres oksydacyjny oraz dysfunkcję mikrokrążenia.
Znaczenie praktyczne diagnostyki funkcjonalnej
Ocena homocysteiny wyłącznie w surowicy krwi nie oddaje pełnego obrazu jej oddziaływania biologicznego. Diagnostyka funkcjonalna umożliwia:
- identyfikację wczesnych zaburzeń metabolicznych,
- ocenę skutków na poziomie komórkowym,
- monitorowanie odpowiedzi na interwencję żywieniową i suplementacyjną,
- personalizację postępowania dietetycznego.
SO/CHECK wpisuje się tym samym w nurt medycyny funkcjonalnej i prewencyjnej, gdzie kluczowe znaczenie ma wykrywanie zaburzeń zanim dojdzie do nieodwracalnych zmian strukturalnych.
Podsumowanie
Homocysteina jest nie tylko parametrem laboratoryjnym, lecz wskaźnikiem integralności metabolizmu jednowęglowego, metylacji i funkcji komórkowych. Jej podwyższenie prowadzi do kaskady zaburzeń obejmujących układ naczyniowy, nerwowy i energetyczny. Diagnostyka SO/CHECK pozwala uchwycić te procesy w sposób funkcjonalny, oferując cenne narzędzie do wczesnej identyfikacji ryzyka i prowadzenia spersonalizowanych interwencji.
Bibliografia
1️⃣ Clarke R, Daly L, Robinson K, et al.
Hyperhomocysteinemia: an independent risk factor for vascular disease.
New England Journal of Medicine. 1991;324(17):1149–1155.
DOI: 10.1056/NEJM199104253241701
🔗 https://pubmed.ncbi.nlm.nih.gov/2011158/
🔗 https://www.nejm.org/doi/full/10.1056/NEJM199104253241701
2️⃣ Wald DS, Law M, Morris JK.
Homocysteine and cardiovascular disease: evidence on causality from a meta-analysis.
BMJ. 2002;325(7374):1202.
DOI: 10.1136/bmj.325.7374.1202
🔗 https://pubmed.ncbi.nlm.nih.gov/12446535/
🔗 https://www.bmj.com/content/325/7374/1202
3️⃣ Selhub J.
Homocysteine metabolism.
Annual Review of Nutrition. 1999;19:217–246.
DOI: 10.1146/annurev.nutr.19.1.217
🔗 https://pubmed.ncbi.nlm.nih.gov/10448523/
🔗 https://www.annualreviews.org/doi/10.1146/annurev.nutr.19.1.217
4️⃣ Refsum H, Ueland PM, Nexo E, et al.
Facts and recommendations about total homocysteine determinations: an expert opinion.
Clinical Chemistry. 2004;50(1):3–32.
DOI: 10.1373/clinchem.2004.036418
🔗 https://pubmed.ncbi.nlm.nih.gov/14602949/
🔗 https://academic.oup.com/clinchem/article/50/1/3/5642079
5️⃣ Humphrey LL, Fu R, Rogers K, et al.
Homocysteine level and coronary heart disease incidence: a systematic review and meta-analysis.
JAMA. 2008;299(17):202–211.
DOI: 10.1001/jama.299.17.202
🔗 https://pubmed.ncbi.nlm.nih.gov/18460696/
🔗 https://jamanetwork.com/journals/jama/fullarticle/182365



