dr hab. Ewa Kłodzińska
Od biofizyki błony do miażdżycy i diagnostyki funkcjonalnej
Komórka jako punkt wyjścia patologii naczyniowej
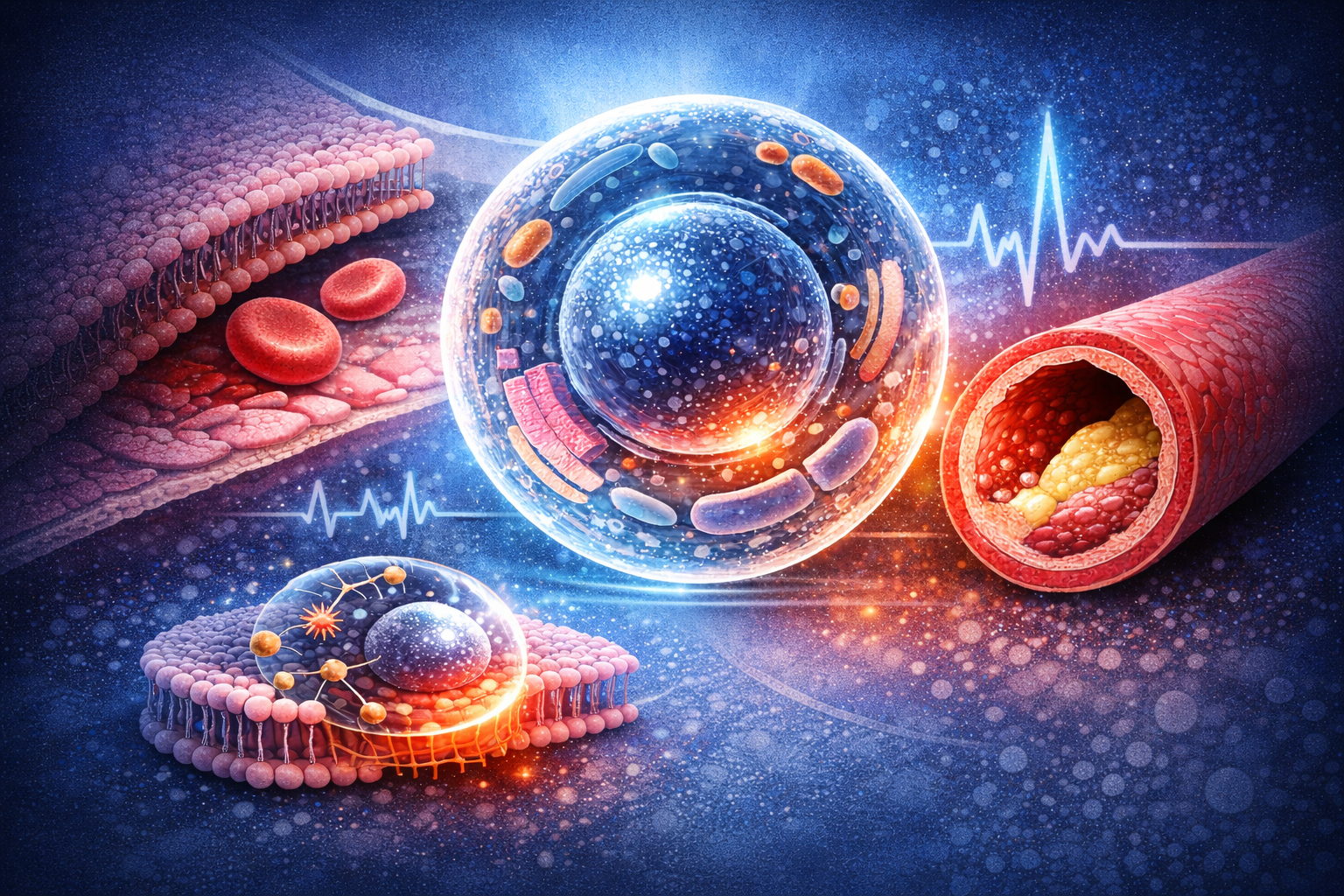
Każdy narząd jest sumą funkcjonujących komórek. Układ sercowo-naczyniowy nie stanowi wyjątku – jego prawidłowe działanie zależy od sprawności komórek śródbłonka, mięśni gładkich naczyń oraz krwinek czerwonych odpowiedzialnych za reologię i mikrokrążenie.
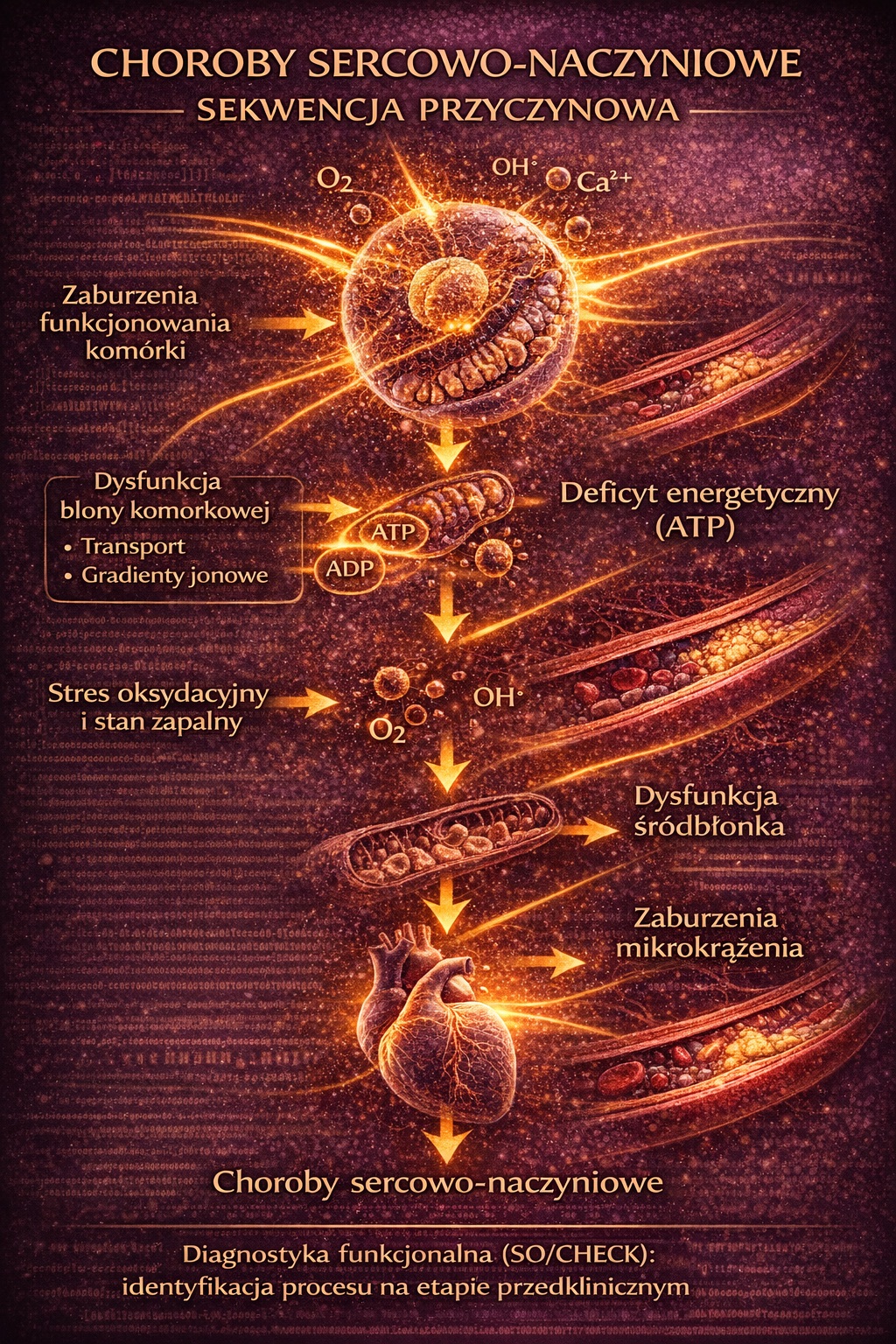
Zaburzenia funkcji narządu są zawsze wtórne wobec zaburzeń komórkowych. W przypadku układu krążenia oznacza to, że zanim dojdzie do nadciśnienia, miażdżycy czy incydentu sercowego, przez lata narasta proces dysfunkcji komórkowej, który pozostaje niewidoczny w klasycznej diagnostyce.
Błona komórkowa – klucz do zrozumienia chorób serca
Centralnym elementem regulującym funkcjonowanie komórki jest błona komórkowa. Nie jest ona bierną barierą, lecz strukturą dynamiczną, odpowiadającą za transport jonów i metabolitów, komunikację międzykomórkową oraz utrzymanie gradientów elektrochemicznych.
Prawidłowa biofizyka błony – jej płynność, ładunek elektryczny i zdolność do utrzymania potencjałów – warunkuje efektywność procesów metabolicznych. Gdy te właściwości ulegają zaburzeniu, transport przezbłonowy staje się mniej wydajny, a komórka zaczyna ponosić coraz większy koszt energetyczny utrzymania homeostazy.
W komórkach śródbłonka oznacza to stopniową utratę zdolności regulacji napięcia naczyniowego, zwiększoną przepuszczalność oraz podatność na aktywację procesów zapalnych.
Energetyka komórki i deficyt ATP
Każda adaptacja biologiczna wymaga energii. ATP jest niezbędne do utrzymania pomp jonowych, naprawy błon komórkowych, regulacji cytoszkieletu oraz kontroli procesów redoks. Przewlekłe zaburzenia biofizyki błony prowadzą do obniżenia efektywności produkcji ATP, co zmusza komórkę do przejścia w tryb przetrwania zamiast regeneracji.
W układzie naczyniowym deficyt energetyczny skutkuje gorszą kontrolą napięcia naczyń, spadkiem rezerwy naczyniowej oraz stopniowym pogorszeniem mikrokrążenia. Na tym etapie zmiany mają charakter funkcjonalny i są potencjalnie odwracalne, choć często nie dają jeszcze jednoznacznych objawów klinicznych.
Stres oksydacyjny jako skutek, nie przyczyna

W klasycznym ujęciu stres oksydacyjny bywa traktowany jako główna przyczyna chorób sercowo-naczyniowych. Tymczasem z perspektywy komórkowej jest on często konsekwencją zaburzeń energetycznych i błonowych. Niedobór ATP oraz przeciążenie metaboliczne prowadzą do narastania reaktywnych form tlenu, które dodatkowo uszkadzają lipidy błonowe i białka.
W śródbłonku skutkuje to zmniejszoną biodostępnością tlenku azotu, nasileniem odpowiedzi zapalnej oraz pogorszeniem funkcji bariery naczyniowej. Powstaje samonapędzające się błędne koło: zaburzona błona → deficyt energii → stres oksydacyjny → dalsze uszkodzenie błony.
Śródbłonek i mikrokrążenie – wczesny etap choroby
Śródbłonek jest pierwszą tkanką, która odzwierciedla długotrwałe zaburzenia komórkowe. Jego dysfunkcja prowadzi do zaburzeń mikrokrążenia – etapu kluczowego, lecz często pomijanego w diagnostyce. Zanim dojdzie do zwężenia dużych naczyń, pogarsza się dystrybucja tlenu i składników odżywczych na poziomie naczyń włosowatych.
Zaburzenia mikrokrążenia tłumaczą wiele niespecyficznych objawów funkcjonalnych, takich jak przewlekłe zmęczenie, obniżona tolerancja wysiłku czy uczucie zimnych kończyn, które często poprzedzają rozpoznanie choroby sercowo-naczyniowej o wiele lat.

Cholesterol i miażdżyca jako adaptacja
W odpowiedzi na przewlekłe uszkodzenia ściany naczyniowej organizm uruchamia mechanizmy adaptacyjne. Jednym z nich jest zwiększone wykorzystanie cholesterolu jako składnika stabilizującego błony komórkowe i strukturę naczyń. Z tej perspektywy blaszka miażdżycowa nie jest punktem wyjścia choroby, lecz końcowym etapem długotrwałego procesu naprawczego, który z czasem traci swoją funkcję ochronną.
Takie ujęcie nie neguje roli lipidów w patogenezie chorób serca, lecz przesuwa akcent z samego efektu końcowego na wcześniejsze mechanizmy, które doprowadziły do konieczności tej adaptacji.
Luka diagnostyczna i potrzeba podejścia funkcjonalnego
Klasyczna diagnostyka sercowo-naczyniowa doskonale identyfikuje zmiany strukturalne i hemodynamiczne, jednak ma ograniczoną zdolność wykrywania etapu funkcjonalnego. Parametry krwi, takie jak lipidogram czy glikemia, odzwierciedlają stan chwilowy i nie zawsze korelują z długotrwałym funkcjonowaniem tkanek.
Tymczasem proces chorobowy toczy się na poziomie komórkowym i tkankowym, zanim stanie się widoczny w obrazie naczyń czy w wynikach laboratoryjnych.
SO/CHECK – diagnostyka funkcjonalna tkanek
W tym kontekście coraz większe znaczenie zyskują narzędzia diagnostyki funkcjonalnej, takie jak SO/CHECK. Metoda ta umożliwia ocenę względnego stanu biochemicznego tkanek, identyfikując wczesne zaburzenia funkcji błon komórkowych, energetyki oraz równowagi metabolicznej.
SO/CHECK nie zastępuje klasycznych badań, lecz je uzupełnia, pozwalając na uchwycenie etapu przedklinicznego – momentu, w którym interwencja może być najbardziej skuteczna i najmniej inwazyjna.
Wnioski
Choroby sercowo-naczyniowe nie zaczynają się w naczyniu ani w sercu. Są one końcowym etapem wieloletnich zaburzeń funkcjonowania komórki, jej błony, energetyki oraz środowiska tkankowego. Zrozumienie tego procesu pozwala przesunąć punkt ciężkości z leczenia powikłań na wczesną prewencję i monitorowanie funkcji układu krążenia.
Podejście komórkowe, wsparte diagnostyką funkcjonalną, otwiera nowy rozdział w myśleniu o chorobach sercowo-naczyniowych – jako procesach dynamicznych, które można rozpoznać i modyfikować na długo przed wystąpieniem nieodwracalnych zmian strukturalnych.
Literatura
- Frąk, W., et al.
Pathophysiology of Cardiovascular Diseases: New Insights into Molecular Mechanisms of Atherosclerosis, Hypertension and Heart Failure.
Biomedicines, 2022.
DOI: https://doi.org/10.3390/biomedicines10081938
PubMed: https://pubmed.ncbi.nlm.nih.gov/36009488/ - Shaito, A., et al.
Oxidative Stress-Induced Endothelial Dysfunction in Cardiovascular Diseases.
Frontiers in Bioscience (Landmark Edition), 2022.
DOI: https://doi.org/10.31083/j.fbl2703105
PubMed: https://pubmed.ncbi.nlm.nih.gov/35345337/ - Higashi, Y., et al.
Endothelial Function and Oxidative Stress in Cardiovascular Diseases.
Circulation Journal, 2009.
DOI: https://doi.org/10.1253/circj.CJ-08-1102
PubMed: https://pubmed.ncbi.nlm.nih.gov/19194043/ - Victor, V. M., et al.
Oxidative Stress, Endothelial Dysfunction and Atherosclerosis.
Current Medicinal Chemistry, 2009.
DOI: https://doi.org/10.2174/138161209789058093
PubMed: https://pubmed.ncbi.nlm.nih.gov/19754375/ - Wang, X., et al.
Endothelial Dysfunction: Molecular Mechanisms and Therapeutic Strategies.
MedComm, 2024.
DOI: https://doi.org/10.1002/mco2.700
PubMed: https://pubmed.ncbi.nlm.nih.gov/39040847/